ワクチンによる臓器破壊:ICD-999「分類不能な医療行為による合併症」
- リンクを取得
- ×
- メール
- 他のアプリ
Twitter(X)上にこういうアホがいた

良い機会なので、ワクチンによる臓器傷害、特に肝臓や腎臓の破壊が、生活上どのように発現するのか、イメージを強める為にも記事にしておく。
1.超過死亡について
ワクチン誘発性のアレルギー疾患で死に至る人物は当然いるだろうが、それが直接の原因とは限らない例も当然ある。重要となるのは「直接原因」と「間接原因」の区別だが、奴等が民衆を欺くことが可能なのは、ワクチンが「間接原因」である例が大半だからに他ならない。例えば鬱で自殺した人間がいたとして、この場合、自殺の直接原因は心理的要因の鬱だが、ワクチンが鬱を誘発したとすれば、ワクチンが自殺を誘導したことになり、即ち間接原因である。現時点ではこれは妄想にしか思えないだろうが、本記事はこれが妄想ではないことを立証するものである。
その本題に入る前に、ワクチンが直接原因となる例の立証に入る。まず、ワクチンで認められる”副反応”はアナフィラキシーだけだと思っているアホが多いが、アナフィラキシーは現在のGell & Coombsアレルギー分類におけるI型アレルギー反応の一種に過ぎず、要するにIgE抗体が関与するアレルギー反応だ。アナフィラキシーの病理からして、これを副反応として認めるということは、ワクチンでアレルギーが生じることを認めることを意味する。従って争点となるのは「アレルギー」の定義である。ではGell & Coombs分類について厚労省の資料を参照しよう。
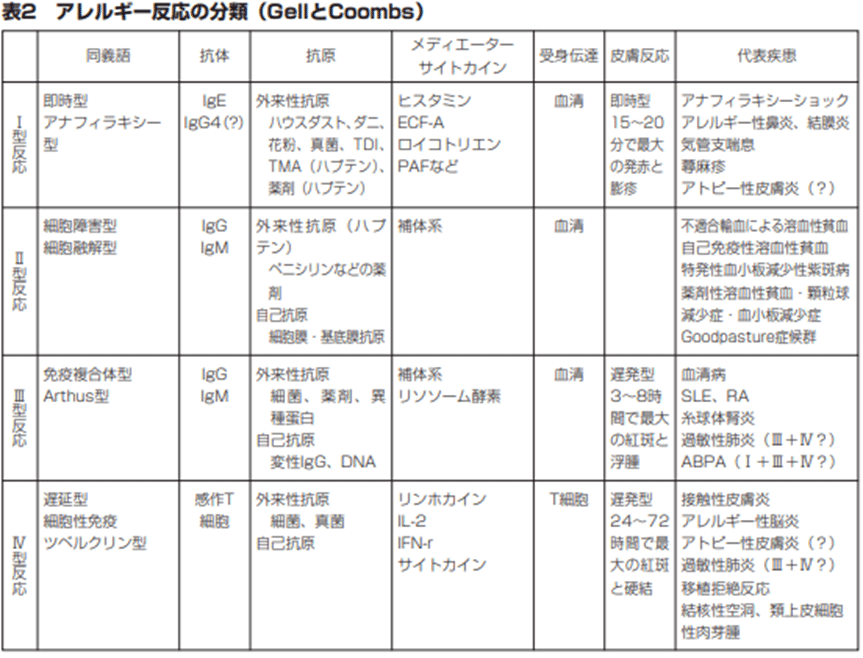
平成22年度リウマチ・アレルギー相談員養成研修会テキスト-第一章アレルギー総論-表2より
さて、I型アレルギーに”IgG4(?)”と表記されているのは何故だろう?厚労省は平成22年(2010年)時点で、IgG4が特定条件下でI型過敏反応を起こす事実を知っていたことになる。
表の通り、これら4つの反応全てが何等かの抗体介在性の過敏反応であり(IV型は無関係なように見えるが後述の通り抗体が関与する)、そしてワクチンの目的は中和抗体(※彼等はIgGと思い込んでいるが、これも完全なイコールではない。他の抗体クラスにも中和活性がある”ものもある”。)の生成である。現在のワクチン推進派の「アナフィラキシーしか副反応として認めない」態度とは要するに「ワクチンに対して生体がIgEを生成した場合しか副反応と認めない」とする歪な主張だ。抗原投与を受けた生体がどの抗体を生成するかなど接種前に予測できるものではない。仮に予測できたとしても、前以て遺伝子検査をしないのは完全なインフォームド・コンセント違反である。
1‐1.全アレルギー反応にIgEは関与する
この時点で因果関係は明白なのだが、今は馬鹿に合わせた話をしているので、10,000歩譲ってIgEの生成のみをアレルギーと定義し、唯一の副反応と認めたとしよう。では他のII~IV型反応にIgEは関与しないのか?この問いは、抗体のクラス(IgE/IgD/IgG/IgA/IgM)で以て過敏反応を分類する現在のGell & Coombs分類は実態を反映しているのか?という問いと同義である。
Descotes, J., & Choquet-Kastylevsky, G. (2001). Gell and Coombs’s classification: Is it still valid? Toxicology, 158(1–2), 43–49. https://doi.org/10.1016/s0300-483x(00)00400-5
「Gell & Coombs分類:まだ妥当であるか?」
GellとCoombsは薬剤アレルギーを四つの病態生理学的タイプに分類した。
1型:アナフィラキシー
2型:抗体介在性細胞傷害反応
3型:免疫複合体介在性反応
4型:遅延型過敏症
である。
この分類は30年以上前に提唱されたにも関わらず、未だに広く使われている。極限られた数の薬剤アレルギー反応をこの分類に当て嵌めた為に、我々の現在の免疫反応に関する理解を反映しておらず、その使用は、特に新たな治療剤の前臨床的安全性評価の文脈では推奨されない。実際、3つの異なる状況、すなわち仮性アレルギー反応、主に抗体媒介反応、細胞媒介反応を同定することができ、これらは現代的でより適切な分類の基礎となりうる。
※この文献はGell & Coombs分類の妥当性は問うているが、本記事のような革命を意図する文献ではない。あくまでこの分類に疑問を投げかける内容であること、メカニズムの図解の為の引用だ。個人的に仮性アレルギーの概念にも懐疑的だ。
1‐1‐1.I型過敏反応
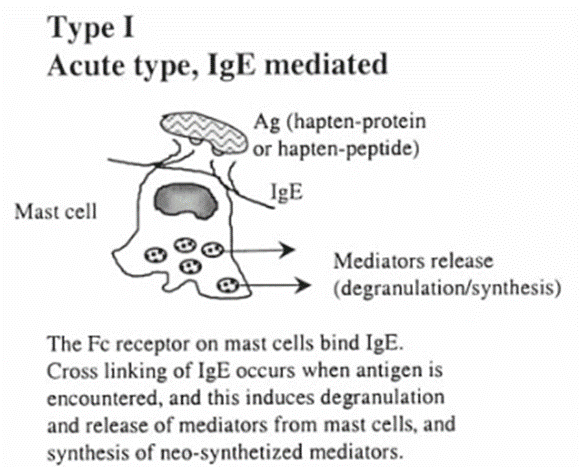
図1(Gell & Coombs分類に基づく外来物質(低分子量の化学物質/薬剤)に対する過敏反応)より。
I型過敏反応:急性型/IgE介在型
肥満細胞(mast cells)上のFc受容体がIgEと結合する。抗原と遭遇してIgEとの架橋が生じると、肥満細胞の脱顆粒(degranulation)が誘発され、メディエイターの放出、新合成メディエイターが合成される。
所謂、狭義のアレルギーがこの反応であり、花粉症やアナフィラキシーがここに含まれる。抗原が体内に侵入し、免疫細胞(※B細胞とは言わない)がIgE抗体を放出する。抗原とIgE抗体が結合した複合体、即ちIgE免疫複合体が肥満細胞や好塩基球の細胞膜上のFc受容体と結合する。するとメディエイター、主にヒスタミンやセロトニンが放出される。特に重要なのがヒスタミンによる血管透過性の上昇だ。血管壁の膜孔がヒスタミンの作用によりこじ開けられる形となり、これにより血管内の成分が血管外に漏出し、痒 みの原因となる。
Gell & Coombs分類ではIgE抗体はこの反応でしか検出されないことになっており、その為「IgE抗体=(狭義の)アレルギー」の認識が生まれることになる。※事実として海外ではAllergyの単語は会話で「花粉症」の意味で使われるらしい。
ここで「IgE免疫複合体」としたのが重要である。免疫複合体immune complexとは「抗原と抗体の結合物」である。そしてそれ以上の定義を持たず、即ち、結合する抗体のクラスは問わない。従って全てのアレルギー反応は本質的に免疫複合体介在性である。後述するが、免疫複合体は抗体単体とは異なる振舞いをするため、別の生理学知識が必要となる。
そして今から立証するのは、このIgE免疫複合体はこの1型アレルギーに限らず、以下3類型のアレルギー反応全てに関与することである。何故IgEの関与が疑われるかだが、宿主がこれら免疫反応による自覚症状を伴うアレルギー症状を経験するには、前提としてヒスタミンによる血管透過性が必要であり、ヒスタミンがそこにいる状況証拠からIgEの存在が示唆される為である。
1‐1‐2.II型過敏反応
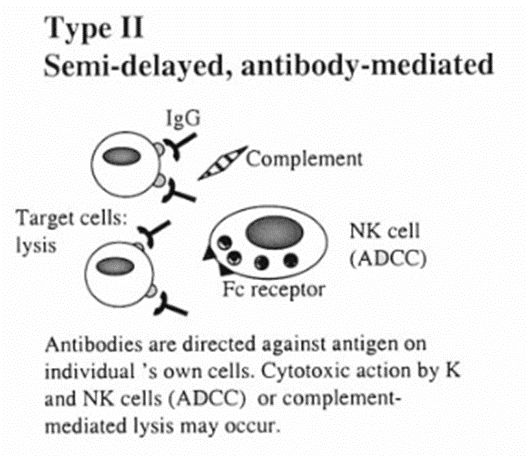
個体自身の細胞上にある抗原に対して抗体が結合する。キラーT細胞やNK細胞による細胞傷害や補体介在性溶解反応が生じる。
1‐1‐3.III型過敏反応
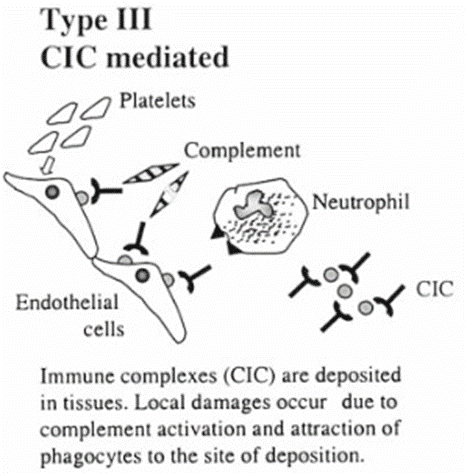
循環性免疫複合体が組織に沈着する。沈着部位での補体活性や貪食細胞の遊走により局所的な損傷が生じる。
1‐1‐4.IV型過敏反応
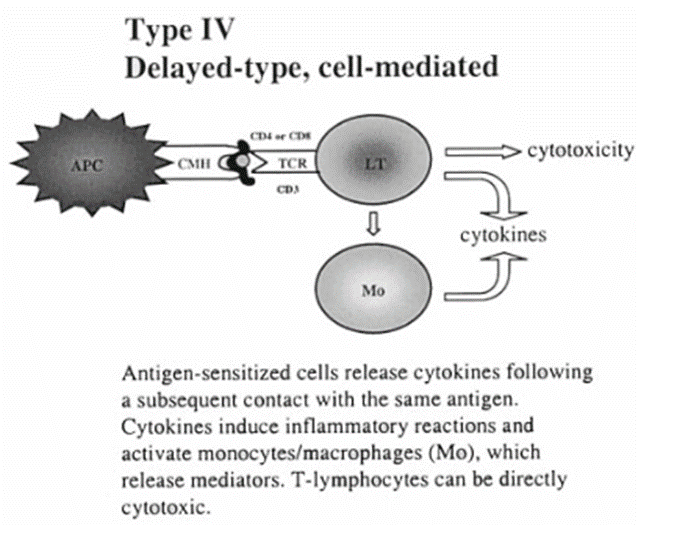
抗原感作細胞は同じ抗原と接触するとサイトカインを放出する。サイトカインは炎症反応を誘発し、単球/マクロファージを活性化し、それによりメディエイターが放出される。T-リンパ球は直接細胞傷害を起こす可能性がある。
解明に困難なのがこちらの4型アレルギー、所謂「遅延型過敏反応」である。別名「ツベルクリン反応型」とも呼ばれ、抗原刺激から24時間以上の長期間の間隔を置いて反応が惹起することに特徴化される。そしてその過敏反応の主役は細胞性免疫であって、液性免疫の抗体が介在しない反応とされる。一部でBCGワクチンが有望視されるのは、抗原である結核菌に対して抗体を介さずに、この遅延型過敏のメカニズムで効率よく細胞性免疫を誘導できると考えられている為だ。自然感染による免疫は細胞性免疫が主役であり、ワクチンの歴史上何かと事故を起こしてきたリスクの高い液性免疫よりも期待値が高くなる所以だ。
この解明が困難を極める理由がここにある。細胞性免疫と液性免疫を誘導するのが各々Th1(CD8+)、Th2細胞(CD4+)と呼ばれるヘルパーT細胞で、このTh1/Th2は互いに抑制関係にあるとされる為であり、この仮説に基づくと、Th1による細胞性免疫が活性化している時点で液性免疫、即ち抗体産生は抑制状態にあることになる。
こうしてみると、一見抗体は関与しないように思われるが、前述の通り皮膚に発現する時点でヒスタミン放出による血管透過性上昇が疑われ、抗原刺激によるヒスタミン放出である以上、IgE介在性が疑われる。従って状況証拠から理論の欠陥が疑われる。何よりこの理論の疑わしい点は、細胞性免疫が主役である点が何故反応の「遅延」を生じさせるかを一切説明しないことだ。中には3日以上後に生じることもある遅延型過敏には明らかにこの”遅延”を制御する因子が別に存在する。この遅延に潜むメカニズムを解明しないことには先に進まない。だとするならやることは唯一つで、免疫学が急速に進歩した1950~70年代から文献を洗い出すことだ。
まず確認すべきは、遅延型過敏反応、即ち4型アレルギーにヒスタミンの上昇は観測されるか否かである。
Inderbitzin, T. (1955). The effect of acute and delayed cutaneous allergic reactions on the amount of histamine in the skin. International Archives of Allergy and Applied Immunology, 7(3), 140–148. https://doi.org/10.1159/000228221
「急性および遅延型皮膚アレルギー反応が皮膚中のヒスタミン量に及ぼす影響」
現在では、実験的な急性アナフィラキシー反応の過程で、組織や血液細胞からヒスタミンが放出されることが確証されている。また、ヒトの蕁麻疹反応では、組織内での抗原抗体相互作用の後、皮膚でヒスタミンが放出されることも認められている。
しかし、遅延性反応(湿疹およびツベルクリン反応)は、ヒスタミンまたはヒスタミン様物質の放出とは無関係であると考えられており、なぜなら、この反応は典型的な血管作用(膨疹の形成と毛細血管透過性の亢進)ではなく、特徴的な炎症性壊死反応を示し、抗ヒスタミン物質はその経過に影響を与えないからである。
遅延型反応における皮膚のヒスタミン含量の変化を記述した実験はないようなので、本研究はこの点を調べるために行われた。
遅延型反応(湿疹反応とツベルクリン反応)と即時型反応(受動的皮膚アナフィラキシーと受動的アルザス反応)に伴う皮膚のヒスタミン含量の変化を比較した。
化学刺激物に対して湿疹反応を起こす予備実験では、ラットはジニトロクロロベンゼンやピクルブルクロライドの感作作用に抵抗性であることが示された。フェレットとモルモットは容易に感作されたが、フェレットの皮膚は技術的な理由で適さないことが判明した。そのため、モルモットに限定した。
どうやら1955年時点で、遅延型過敏反応にヒスタミンは無関係だと”考えられて”いたようだ。その根拠が、抗ヒスタミン剤でアレルギー反応が阻害できなかった為らしい。その事実から、そもそもヒスタミンを計測する発想にすらならなかったと見受けられる。この実験で、実験的アナフィラキシー反応(1型アレルギー)、アルザス反応(55年時点で2型分類)、湿疹反応(血清病腎炎による湿疹:3型)、ツベルクリン反応(遅延型の4型)の経過中における皮膚切片中のヒスタミン量を計測した。今回知りたいのは遅延型過敏反応の為、ツベルクリン反応に限定する。その結果が以下の表の通りである。
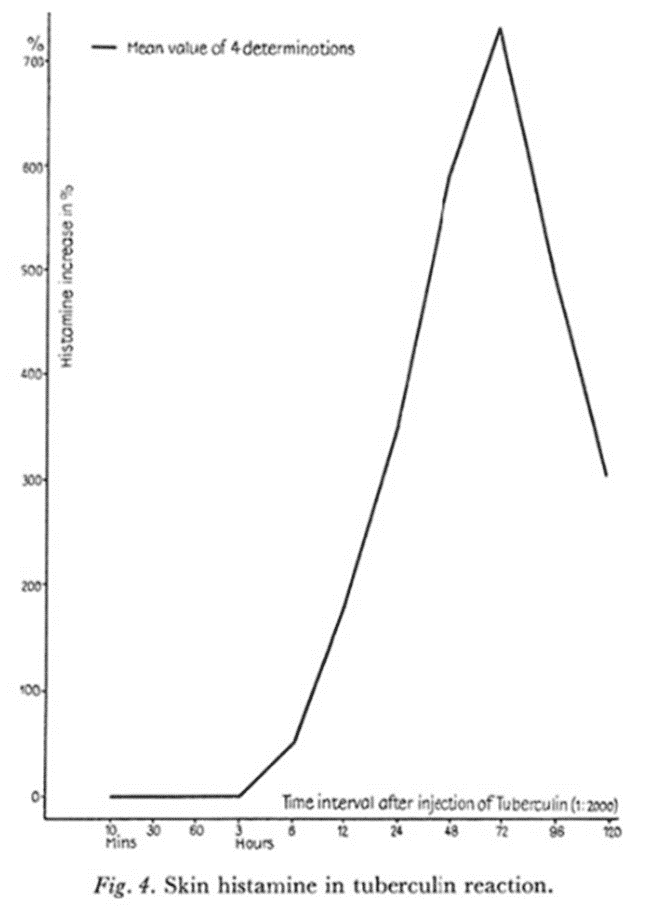
つまり、症状出現に一致しておよそ7倍のヒスタミン量が検出された。これで遅延型過敏反応にもヒスタミン上昇は観測されることが判明した。しかし予想に反してヒスタミンは直接血管透過性には関与しなかった。だから遅延型過敏で抗体の関与が議論されてこなかったのだろうが…問題ない。発疹の発現経路には、ヒスタミン以外に、プ ロ ス タ グ ラ ン ジ ン 経 路がある為だ。抗ヒスタミン剤で阻害されずとも不思議ではない。
Morley, J., Beets, J. L., Bray, M. A., & Paul, W. (1980). Regulation of allergic responses by prostaglandins: A review. Journal of the Royal Society of Medicine, 73(6), 443–447.
「プロスタグランジンによるアレルギー反応の制御:総説」
プロスタノイド(エンドペルオキシド、古典的プロスタグランジン、トロンボキサン、プロスタサイクリン)はかなりの生物学的効力を持つ内因性物質である。これらの物質は不飽和脂肪酸の代謝により形成される(図1)。十分に確立されたプロスタグランジン(PGs)の特性には強力な血管運動活性があり、消化器、気管支、泌尿系の平滑筋に作用する他、血小板系にも作用する(Horrobin 1978)。こうした薬理学的プロフィールから、これら化合物がアレルギー反応のメディエイターとして注目を浴びるのは恐らく必然であった。例えば、プロスタグランジンが皮膚アナフィラキシー(Williams & Morley 1973)の局所反応、1型過敏反応(Piper & Vane 1971)における抗原チャレンジ後の気管支収縮や、腸アレルギー(Buisseret et al. 1978)における透過性の変化に関与する可能性が示唆されている。
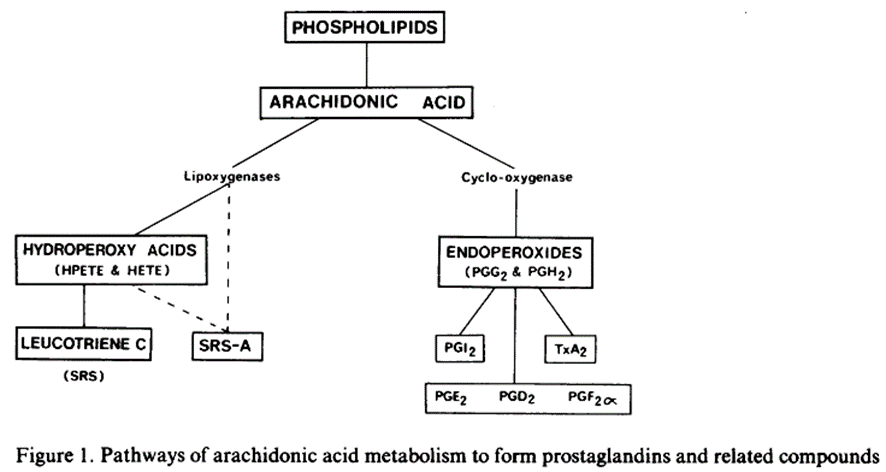
リン脂質⇒アラキドン酸⇒
①リポキシゲナーゼ⇒ヒドロペルオキシ酸⇒ロイコトリエンC
②シクロオキシゲナーゼ⇒エンドペルオキシド
⇒2-1:PGI2、
2-2:PGE2/PGD2/PGF2α、
2-3:TxA2
1‐2.免疫複合体の生理学
では、ワクチンという名の抗原注射によって何が生じるかというと当然抗体反応が生じる。そして抗原と抗体の結合物を免疫複合体Immune Complexと呼ぶ。先ほどの厚労省の資料を再確認しよう。
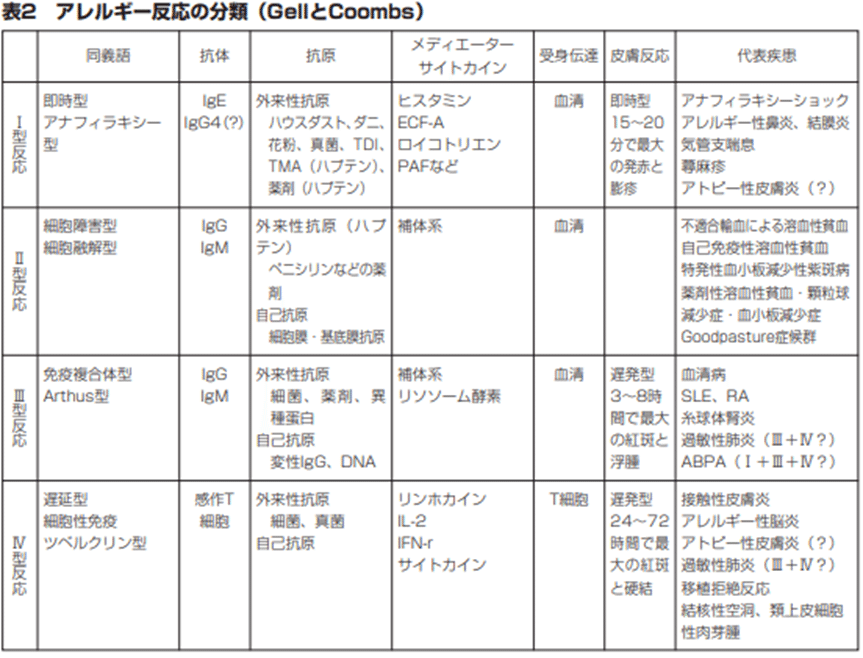
この表を見ると、免疫複合体はIII型反応にしか関与しないように思われる。だが繰り返すが「免疫複合体」は「抗原と抗体の結合物」以上の定義を持たない。即ち、結合した抗体のクラス(IgE/IgD/IgM/IgG/IgA)に関係なく、その複合体は全て定義上免疫複合体であり、そして上述の通りI~IV型反応全てが抗体介在性反応であることから、I~IV型反応の全てが免疫複合体型である。だからこそ、「アレルギー」の産みの親であるクレメンス・ピルケは「抗原と抗体の衝突(Collision)による疾患」を総称して「血清病serum sickness」と命名したのであり、故に血清病をIII型のみに限って分類すること自体が隠蔽である。以上より、「I~IV型アレルギー」=「免疫複合体疾患」=「血清病」の図式が完成し、実験室場面ではその発症部位により区別される。
梁瀬恵子.(1980). 免疫複合体とその意義について. 皮膚,22(4),517–531. https://doi.org/10.11340/SKINRESEARCH1959.22.517
IC(Immune complex)がある種の疾患の病因となり得るとの推測は古くからなされ、Von Pirquet(2)はすでに60年以上前にヒトの血清病における血管、腎、心、皮膚、関節の病変の原因として異物の中の抗原と患者の対応する抗体との結合物、すなわちICが有毒物質を産生するためと考えた。このようなスペキュレーションに対しての実験的な裏付けは1950年代になってから著しく発展し、IC疾患の実験モデルとして局所性のものはArthus現象、全身性のものは実験血清病として示されるようになった。
そしてこの免疫複合体、タンパク質同士の複合体であるため、固体であるかのように錯覚する。しかし、Merck Manualに記載の通り、免疫複合体には可溶性Solubleの形態が存在する。可溶性が存在するなら不溶性Insolubleも存在する。では両者の違いとは何か?
Carter, P. M. (1973). Immune complex disease. Annals of the Rheumatic Diseases, 32(3), 265. https://doi.org/10.1136/ARD.32.3.265
「免疫複合体疾患」
複合体形成
急性血清病は抗原過剰域の存在下で形成される比較的小さな複合体の沈着により生じる全身性疾患である。単回の抗原チャレンジ後の過敏症であり、投与後7~14日後に発症する。馬血清を例に、大量の抗原の単回注射後に形成される可溶性複合体soluble complexを図1に示す。
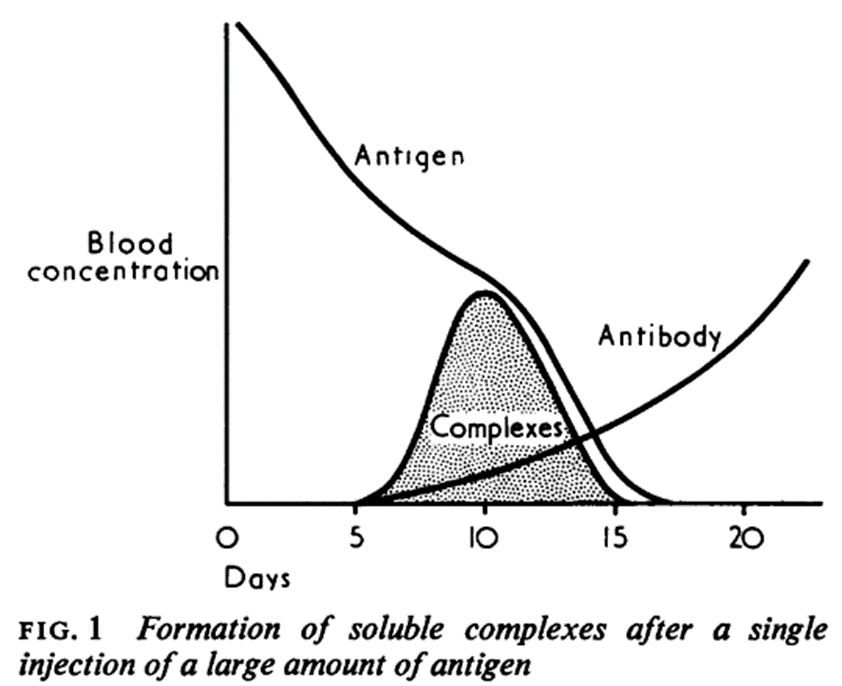
しかし、急性および慢性血清病は、抗原チャレンジが繰り返された後、循環する抗原が新しく形成された抗体と結合するまでの短期間、あるいは長期間にわたって低濃度の複合体が形成された後に起こる可能性がある。(Dixon, Vasquez, Weigle, and Cochrane, 1958; Germuth, Senterfit, and Pollack, 1967b).
アルザスArthus反応とは、過剰に免疫化された動物に可溶性抗原を注射した数時間後に生じる局所的な紅斑と浮腫の形成であり、総体的な抗体過剰域の存在下での巨大な免疫複合体の形成に起因する。血清病とアルザス反応は臨床的には異なるものの、複合体のサイズと組成、沈着部位で区別される、スペクトラム状の免疫複合体疾患における異なる段階と考えるのが最適であろう。これらの因子は経時的に変化し、血清病とアルザス反応の両方の特徴は、単一疾患プロセスの異なる段階で見られる可能性がある。如何なる複合体であろうと、その組成により溶 解 度が変化する。このことは、オバルブミンと抗オバルブミンの沈殿曲線が示している。
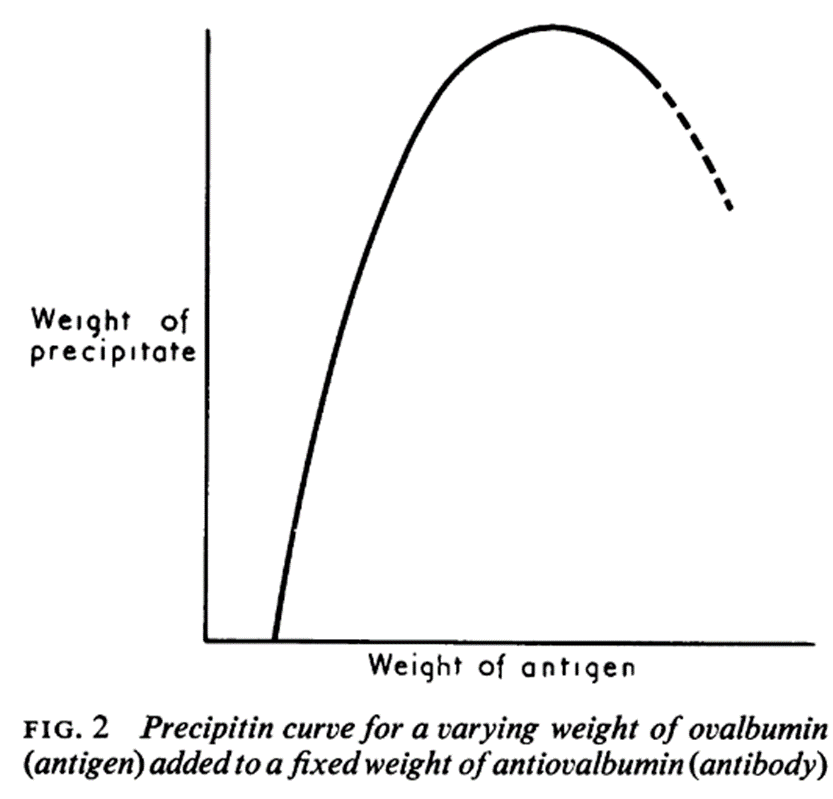
抗原過剰域の複合体は、抗体過剰域の複合体より相対的に溶 解 度 が 高 く、総体的な抗体過剰域の複合体が急速に沈殿し、注射部位に局所化する傾向にある一方で、抗原過剰域の可溶性複合体は全身性疾患を起こす可能性がある。
in vitro研究により、循環系の可溶性複合体、遊離抗原、不溶性複合体、微量の遊離抗体との間に平衡状態が存在することが示唆されている(Germuth, Keleman, and Pollack, 1967a)。この平衡状態は複合体の全体公式で表現可能である。
xAg2Ab⇔(Ag3Ab2)x⇔(AgAb)x⇔(AgAb2)x⇔(AgAb3)x
これは以下のように簡略化可能であろう。
可溶性複合体⇔不溶性複合体
免疫複合体疾患は、特に抗原チャレンジへの反応として低親和性抗体の産生が生じた場合に発症することが示唆されている(Soothill and Steward, 1971)。この結果、まず抗原の不完全な免疫除去が生じ、その後に少量の高親和性抗体も産生される可能性はあるものの、それは持続的な抗原過剰域の中で生成される為、溶解性の高い複合体を形成する可能性が高い。

●全身性
関節リウマチ
全身性エリテマトーデス
溶連菌感染後腎炎
マラリア腎炎
ペニシリン過敏症
●局所性
農夫肺
鳩飼育者肺
結節性紅斑
虫刺され
麻疹後脳炎
風疹関節炎
要約すると
・急性血清病とは、抗原の割合の多い(抗原過剰域)微小な免疫複合体の形成に起因する、抗原投与から7~14日の間隔を置いて発症する全身疾患である
・抗原の頻回投与により、低濃度の複合体が長期間に亘り循環する慢性血清病に移行する
・アルザス反応とは、その頻回投与により、抗体の割合の多い(抗体過剰域)巨大な免疫複合体形成に起因し、注射部位への局所化を特徴とする
・血清病とアルザス反応は、臨床症状が異なるだけの同一疾患と見做すべきである
・抗原過剰域複合体は溶解性を呈して全身循環し、抗体過剰域複合体は不溶性を呈して局所に沈殿する
・血清病の発症期間中は遊離抗原、可溶性複合体、不溶性複合体、遊離抗体の全てが血液中に平衡状態、つまりこれら全てが均衡を保ちながら同時に循環する
反論としては、実験血清病(実験室での免疫複合体疾患)に使用される抗原はBSA(牛血清アルブミン)や馬血清の話であって、ワクチンとは無関係だと言われるかもしれない。そして血清病は抗原と病変部位との間に免疫学的関連のない解剖学的疾患、即ち人体の構造上の疾患だと言おうと理解できないアホがいそうだが、だったら教えて欲しい。何故SARS-CoV2スパイクタンパク質の可溶性免疫複合体soluble immune complexが存在するのか?
2.帯状疱疹の増加について
帯状疱疹ウイルス
3.交通事故について
4.若者の自殺増加について
5.犯罪件数について
ワクチンと犯罪…一見無関係に見えそうだ。犯罪の種類にも寄るが、昨今の殺人事件に絞ろう。件数自体は昭和から減少傾向にあると聞くが、現代の殺人は少年犯罪が多い傾向にあるらしい。センセーショナルに報道するせいで目立っているだけにも思えるが、では犯罪衝動=攻撃性の増加と捉えよう。
代替療法界隈はMg不足だと騒ぐが、彼等は基本的にMgとZn、Vitamin A/C/D/Kで全てが解決すると思っているフシがあるし、その原因が農薬と添加物、水道水の塩素/フッ素による「質の栄養不足」、或いは屋内で過ごす時間の増加で日光不足だとしか言わない。現代のインフラが日当たりにどれだけ技術を注いでいるかも知らず、水道水の塩素/フッ素が何の感染症対策の為かも知らずに何百年と同じことを言い続けている一切成長のない界隈である。
では人間の攻撃性を決定するのは何か?その参考文献として、以下に勝るものはないと考える。
Paul F, B., & David, B. (1981). The Biology of Aggression. NATO Advanced study institutes series.
「攻撃性の生物学」
6.米麹について
- リンクを取得
- ×
- メール
- 他のアプリ
コメント
コメントを投稿